氢原子与碱金属原子
氢原子
氢原子的定态 Schrodinger 方程
- 定态 Schrodinger 方程:
- Laplace 算子:
- 分离变量: ψ(r, θ, φ) = R(r)Θ(θ)Φ(φ)
Θlm(θ) = APlm(cos θ), l = 0, 1, 2, …, n − 1 6. 径向部分:
- 主量子数
和能级: Ĥ 的本征方程: Ĥψnlm(r, θ, φ) = Enψ(r, θ, φ)
能级:
能级的简并度(同一能级,氢原子有n2个本征态):
- 角量子数
和轨道角动量: L̂2 的本征方程: L̂2Ylm(θ, φ) = l(l + 1)ℏ2Ylm(θ, φ)
轨道角动量的大小:
- 磁量子数
和轨道角动量空间取向: L̂z 的本征方程: L̂zYlm(θ, φ) = mℏYlm(θ, φ)
轨道角动量
分量的大小: Lz = mℏ, m = 0, ±1, ±2, …, ±l
电子概率密度分布
空间概率分布: |ψnlm(r, θ, φ)|2|dτ| = |Rnl(r)|2|Ylm(θ, φ)|2r2sin θdrdθdφ
角向概率分布: Plm(θ, φ)dΩ = ∫0+∞|Rnl(r)|2r2dr|Ylm(θ, φ)|2sin θdθdφ = |Ylm(θ, φ)|2dΩ
径向概率分布: Pnl(r)dr = ∫02πdφ∫0π|Ylm(θ, φ)|2sin θdθ|Rnl(r)|2r2dr = Rnl2(r)r2dr
Pnl(r) 有
个极大值点, 个极小值点。主峰位置随 增加向原子核移近。 值越小,最内层的峰离核越近,说明对同一 值,随着 的减小,电子出现在原子核附近的概率逐渐增大。 电子径向坐标的平均值:
定态的宇称
空间反演算符: P̂ψnlm(r, θ, φ) = ψnlm(r, π − θ, φ + π)
氢原子定态的宇称取决于
: Ylm(π − θ, φ + π) = (−1)lYlm(θ, φ) P̂ψnlm(r, θ, φ) = (−1)lψnlm(r, θ, φ)
跃迁的选择定则
感生偶极矩算符: D̂ = −er
电偶极跃迁矩阵元: Dnn′ = ∫−∞+∞ψn*(r)D̂ψn′(r)dτ
在 $ n(r)
{n’}(r) |D_{nn’}|^2 $。 发生电偶极辐射跃迁的条件
⟨erij⟩ = e⟨j|r|i⟩ = e∫−∞+∞ψn2l2m2*rψn1l1m1 ≠ 0
- 方位角部分: x : ∫02π[ei(m1 − m2 + 1)φ + ei(m1 − m2 − 1)φ]dφ y : ∫02π[ei(m1 − m2 + 1)φ − ei(m1 − m2 − 1)φ]dφ z : ∫02πei(m1 − m2)φdφ
磁量子数的选择定则: Δm = m2 − m1 = 0, ±1
- 极角部分:
角量子数的选择定则 (Laporte 选择定则): Δl = l2 − l1 = ±1
碱金属原子
碱金属原子能级的粗结构:
- 对同一主量子数
,碱金属能级位置低于氢原子。 - 对同一主量子数
,不同角量子数 导致能级分裂。
- 对同一主量子数
碱金属原子能级低于H的原因:
- 原子实极化:价电子对原子实有极化作用。
- 轨道贯穿:价电子有一定概率出现在原子实内。
原子实的有效电荷数𝑍∗ > 1,使得碱金属原子能量降低.(用量子力学的观点就是价电子的波函数在原子实内部不为零)
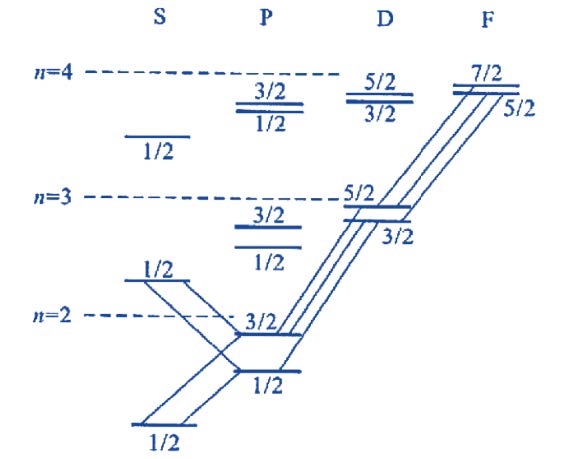
碱金属原子的能级和光谱项:
不同能级之间的跃迁遵守电偶极跃迁规则. 跃迁前后角量子数𝑙 的变化满足Δ𝑙 = ±1. 图中由𝑛𝑝 向2𝑠 跃迁的,即𝑛𝑝 → 2𝑠 为主线系,𝑛𝑠 → 2𝑝 为第二辅线系,𝑛𝑑 → 2𝑝为第一辅线系,𝑛𝑓 → 3𝑑 为柏格曼系. 2𝑝 向基态2𝑠 的跃迁产生的谱线称为共振线.
电子的自旋与磁矩
电子轨道的磁矩
电子轨道的磁矩:
电子轨道的磁矩的大小:
电子轨道的磁矩
分量的大小:
Stern-Gerlach 实验
作用于原子磁偶极矩上的力:
横向位移:
电子自旋的磁矩
电子自旋角动量量子数:
电子自旋角动量:
电子自旋角动量的大小:
电子自旋角动量
分量的大小:
电子自旋的磁矩:
电子自旋磁矩和自旋角动量的关系:
电子自旋磁矩的大小:
电子轨道和自旋磁矩的公式:
电子量子态的波函数: ϕnlmms = ψnlm(r, θ, φ)χms(sz)
碱金属原子光谱的精细结构
原子的总角动量
原子的总角动量: 𝒥 = ℒ + 𝒮
总角动量的大小:
总角动量
分量的大小: 𝒥z = MJℏ, MJ = 0, ±1, …, ±J ℒ𝒮 耦合不改变碱金属原子量子态的数目:
自旋-轨道相互作用
自旋 − 轨道耦合 使得 同一l能级进一步分裂为两个值 (能级精细结构)
j 值大的能级高, j 值小的能级低
s 态不分裂
原子实在电子处产生的磁感应强度:
在原子实静止系中,Thomas 给出右面应乘 1/2:
自旋-轨道耦合能:
自旋-轨道耦合能在原子定态中的平均值:
碱金属原子光谱的精细结构
碱金属原子总能量: Enlj = Enl + ΔEls
双重能级:
双重能级间隔:
波数间隔:
精细能级跃迁的选择定则: ΔJ = 0, ±1, Δl = ±1
原子能级符号: n2S + 1LJ
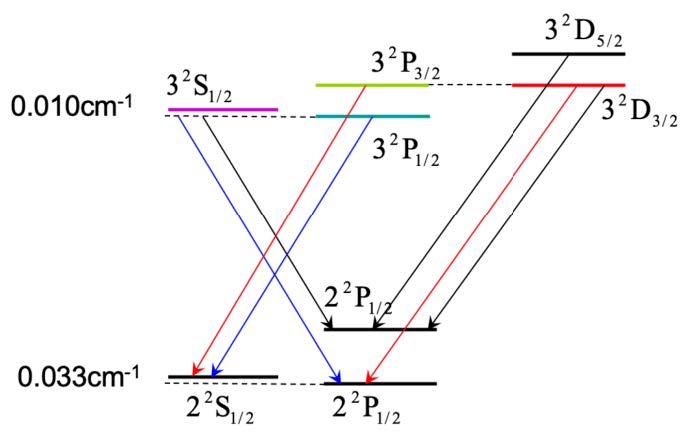
图 1: 锂原子能级能级的精细结构及允许跃迁
### 碱金属原子能级精细结构的几个特点: 1. 双重能级分裂的大小与有效核电荷数𝑍∗ 的四次幂成正比,随着原子序数的增大,𝑍∗ 也增大,所以高原子序数Z 的原子双重能级分裂大. 2. n2S1/2能级不存在精细分裂,因为𝑙 = 0 时,不存在轨道运动产生的磁场,但通常 仍保留多重数为2 的标记.S 3. Δ𝐸𝑙𝑠 反比于𝑛3 和𝑙3,对同一原子,随着量子数𝑛 及𝑙 的增大,精细分裂迅速减小. 4. 双重能级中,具有较高J 值的能级,能量较高.